LuTX24.DE
und dann? nach der OP?
Direkt nach der Operation liegt der Patient normalerweise ca. 7-10 Tage in der Intensivstation. Von dort geht es dann in eine normale Krankenstation. Von Beginn an wird der Patient dann mobilisiert, bekommt Physiotherapie.
Die Verläufe sind allerdings sehr unterschiedlich, denn immerhin handelt es sich bei einer Lungentransplantation um eine der aufwändigsten Operationen überhaupt, die für den gesamten Organismus in jedem Fall eine erhebliche Herausforderung bedeutet.
Hygiene
Wegen der Immunsuppression ist nach der Transplantation auf gute Hygiene zu achten. So gehört Körperpflege zu den wichtigen Dingen, die zu erledigen sind. Dazu gehören regelmässige Körperreinigung inklusive Mundhygiene, häufiger Wäschewechsel, prinzipiell Vermeidung von Stäuben, Schmutz, etc.
Auch Haustiere sind hier zu nennen, da diese in der Regel sowohl Krankheitskeime tragen und verbreiten können und auch ansonsten die Staubbelastung innerhalb einer Wohneinheit erheblich vergrössern. Nicht selten ist die Vorerkrankung vor der LTPL auf die vorherigen hygienischen Umstände zurückzuführen. Diese gilt es nun dringend zu vermeiden.
Gartenarbeit muss dringend vollständig vermieden werden. Es darf kein Rasen mehr gemäht und keine Hecke mehr geschnitten werden. Durch die Immunsuppression können Pilzsporen eingeatmet werden, die dann die neue Lunge befallen und sich hier ausbreiten. Durch Inhalationen zum Beispiel mit Ampho wird davor prophylaktisch geschützt.

Ernährung
auch hier gilt das Vorgenannte! Hygiene! Das Essen soll weitestgehend keimfrei sein. Grundsätzlich kann alles gegessen werden, was gekocht ist, denn durch den Kochvorgang werden aktive Keime abgetötet. Das bedeutet, dass Eier immer HART gekocht sein müssen. Ein weicher Dotter könnte Keime wie Salmonellen enthalten. Fleisch darf innen nicht mehr blutig sein, deshalb Vorsicht bei Filet und anderen Spezialitäten. Aber auch Rohwürste wie Salami oder roher Schinken sind ab jetzt Tabu! Beeren ebenfalls, da diese auf der Schale Pilzsporen tragen können und nicht geschält werden können.
Ebenfalls darf keine Eiskugel mehr verzehrt werden, da hier ebenfalls die hygienischen Anforderungen nicht gegeben sind. Rohmilchkäse kann auch Keime enthalten, daraus folgt, keine Schimmelkäse wie Gorgonzola, kein Camenbert, Vorsicht bei Mozarella. Alle Käse die pasteurisiert sind, können hingegen gegessen werden.

Bewegung und Sport
Durch die neue Lunge ist es nun wieder möglich, sich ausgiebig zu bewegen. Allerdings ist in der Regel durch die teilweise langjährige Vorerkrankung ein deutlicher Muskel- und Konditionsabfall eingetreten, den es nun gilt wieder abzubauen. Hier bietet es sich an, auf einem Smart-Phone oder ähnlichem Gerät (Smartwatch, Fitnessarmband) die eigene Bewegung aufzuzeichnen und diese auch zu dokumentieren, mit dem Ziel, seine Leistungsfähigkeit wieder zu steigern.
Auch gymnastische Übungen, Ergometer, leichte Gewichtshanteln, viele Spaziergänge - gerne auch mal mit Umwegen - bieten sich hier an. Dabei ist es manchmal erforderlich, überhaupt die Atemmuskulatur wie das Zwerchfell wieder zu trainieren. Denn durch die Vorerkrankung hat auch die Atemmuskulatur teilweise erheblich abgebaut. Fibrotiker beispielsweise atmen im Endstadium nur noch in den oberen Teil der Lungen, da der untere bereits unbrauchbar ist. Dieses neue Atemlernen wird von vielen Betroffenen als grosse Herausforderung empfunden!

Vitalwerte
Die Dokumentation der Vitalwerte wie FEV1 Wert, Sauerstoffsättigung, Blutdruck, Puls, Gewicht soll dem Patienten und auch den behandelnden Ärzten die Möglichkeit geben, den Zustand des Patienten genau im Blick zu haben, so dass eine Verschlechterung kurzfristig erkannt werden kann und darauf sofort reagiert werden kann. Denn wenn schnell reagiert wird, so kann schnellstmöglich gehandelt werden und somit Schlimmes vermieden werden. Diese Disziplin, die der Patient aufbringen muss, gilt als seine Lebensversicherung. Statistiken zeigen, dass die Einhaltung dieser Disziplin tatsächlich zu besseren Ergebnissen führt.

Rehabilitation
Nach dem Krankenhaus Aufenthalt folgt in der Regel auf Wunsch eine Reha von mindestens drei Wochen, die problemlos ein-
bis zweimal verlängert werden kann. Hier werden durch körperliche Betätigung, Spiele und Vorträge die Betroffenen
auf die neue Situation vorbereitet. Zur Zeit gibt es in Deutschland nur zwei REHA Zentren, die Lungentransplantierte betreuen: es ist die
die Klinik Martinusquelle in Bad Lippspringe (NRW) und die
Schön Klinik im Berchtesgadener Land. Das es nur zwei Kliniken sind, liegt
darin begründet, dass die Versorgung der Lungentransplantierten einer besonderen Aufmerksamkeit und Hygiene bedarf!

Austausch mit anderen
Durch die langen Krankenhausaufenthalte entstehen in der Regel Freundschaften, da nun zum erstenmal Mitpatienten über einen längeren Zeitraum getroffen werden. Dieser Austausch kann sehr fruchtend sein, da jeder LTXler dasselbe Ziel verfolgt: seine Leistungsfähigkeit zu steigern und wieder vollständig genesen in die Gesellschaft zurückzukehren. Man hilft sich beim Erreichen der Ziele, weiss aber auch genau, welche Schmerzen, welche Schwächen der oder die andere haben kann. So kann vertrauensvoll miteinander umgegangen werden.

Lungentransplantation
Die Lungentransplantation (LTX, LUTX oder LTPL) ist eine Behandlungsform für fortgeschrittene Lungenkrankheiten
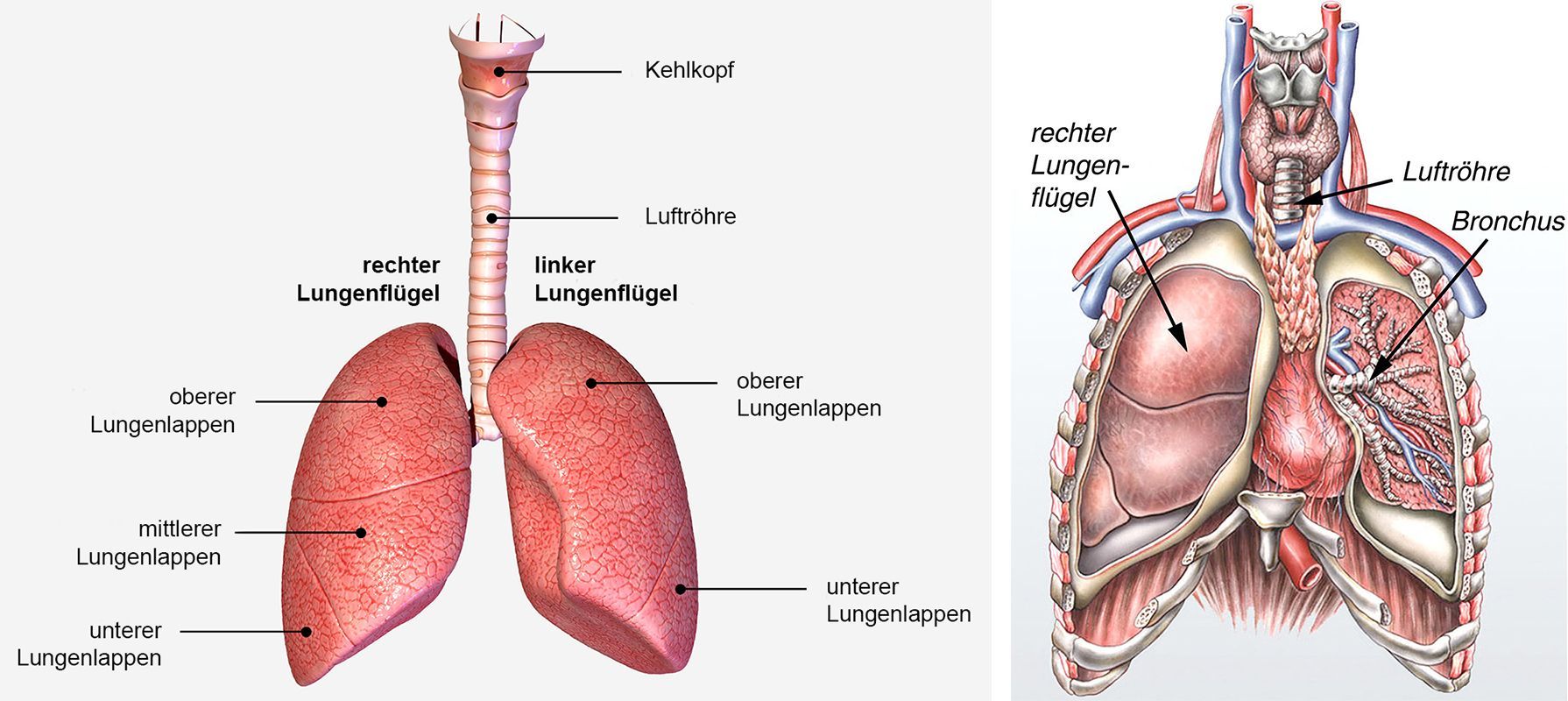
und besteht in der Transplantation eines Lungenflügels (Einzellungentransplantation), beider Lungenflügel
(beidseitige Lungentransplantation) oder nur eines oder mehrerer Lungenlappen von einem Organspender zu einem Empfänger.
Die Herz-Lungen-Transplantation, das heißt die Transplantation beider Lungen zusammen mit dem Herzen, wird
heute nur noch selten – vor allem bei Patienten mit Herzfehlern – durchgeführt. Seit einigen Jahren besteht auch vor allem für lungenkranke Kinder die Möglichkeit einer sogenannten Lebend-Lungentransplantation (englisch living-related lung transplantation), das heißt die Verpflanzung je eines Lungenlappens von zwei lebenden Spendern auf einen meist sehr jungen Empfänger.
Geschichte
Seit den 80er-Jahren hat sich die Lungentransplantation von einer experimentellen Technik zur etablierten
Behandlungsmöglichkeit schwerer Erkrankungen der Lungen und des Lungenkreislaufes entwickelt. Diesen Fortschritt haben vor allem die verbesserte Operationstechnik und Organpräservation, die genaueren Selektionskriterien sowie eine verfeinerte Diagnostik, Prophylaxe und Behandlung von Abstoßungsreaktionen und Infektionen ermöglicht.
Das Ziel aller Bestrebungen ist jedoch nach wie vor die Verringerung von Erkrankungshäufigkeit und Sterblichkeit infolge des sogenannten Bronchiolitis-obliterans-Syndroms (BOS), das nach wie vor die Langzeitresultate der Lungentransplantation am meisten beeinträchtigt.
In den 1940er Jahren führte der russische Chirurg Wladimir Demichow bei Hunden über 100 experimentelle Herz-Lungen-Transplantationen ohne Herz-Lungen-Maschine oder Immunsuppression durch. Er konnte zeigen, dass diese transplantierten Organe die Versuchstiere zumindest über eine kurze Zeit am Leben erhalten konnten.
Diese Resultate wurden von Dominique Métras 1950 in Frankreich und Hardin 1954 in den USA bestätigt. In der Folge – insbesondere dank der Einführung der Herz-Lungen-Maschine durch Webb – gelang James D. Hardy 1963 die erste einseitige Lungentransplantation beim Menschen. Der Patient überlebte jedoch nur 18 Tage. Bis 1980 wurden insgesamt 3 Herz-Lungen- und 38 Einzellungentransplantationen bei Menschen durchgeführt. Mit der Ausnahme einesPatienten, der 10 Monate überlebte, starben alle innerhalb von drei Monaten.
Mit der Einführung des Ciclosporins im Jahre 1981 begann eine neue Ära der Transplantationschirurgie einschließlich der LTPL. Im März 1981 gelang Bruce Reitz in Stanford die erste längerfristig erfolgreiche Herz-Lungen-Transplantation. Die weiteren technischen Entwicklungen der isolierten Lungentransplantation waren vor allem geprägt durch die Arbeiten von Joel Cooper und Mitarbeitern in Toronto und später in St. Louis. Diese Gruppe führte 1983 die erste Einzel-Lungentransplantation, 1986 die erste En-bloc-Doppel-Lungentransplantation und 1989 die erste sequentielle beidseitige Lungentransplantation durch.
1993 war es Vaughn Starnes vom Stanford Medical Center, der als erster Chirurg eine Lungentransplantation unter lebenden Verwandten ausführte. Er nahm je einen Lungenflügel des Vaters und der Mutter und verpflanzte sie der 12-jährigen Tochter.
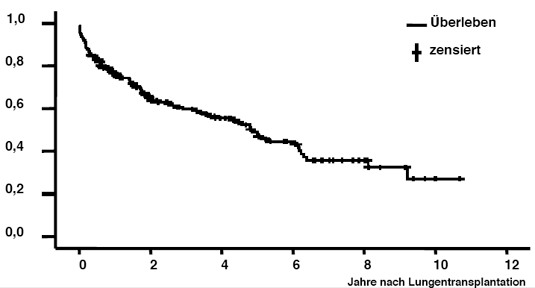
Bis Mitte 2005 wurden weltweit über 18.000 Lungentransplantationen, davon etwa die Hälfte Einzel-Transplantationen, durchgeführt. Die mittlere Ein- beziehungsweise Fünfjahresüberlebensrate beträgt weltweit insgesamt 70% beziehungsweise 50%. Einzelne Zentren erreichen jedoch mittlerweile ein Fünfjahresüberleben von etwa 80%.
Es gibt mehrere Fälle von zweiten, dritten und sogar vierten Lungentransplantationen in Deutschland, wobei Patienten durchschnittlich alle fünf Jahre auf einen neuen Lungenspender angewiesen sind.
Transplantationszentren
In Deutschland können nur wenige Krankenhäuser Lungen transplantieren. Die meisten Lungentransplantationen werden am Klinikum der Medizinischen Hochschule Hannover durchgeführt; an zweiter Stelle steht das Klinikum der Universität München gemeinsam mit der Ruhrlandklinik in Essen.

In Österreich ist das AKH Wien Lungentransplantationszentrum mit mehr als 100 Transplantationen pro Jahr. Von 1989 bis Anfang 2018 war Walter Klepetko Leiter des Lungentransplantationsprogramms.
In der Schweiz existieren zwei Zentren: dasjenige für die Deutschschweiz am Universitätsspital Zürich (USZ) und das Centre Romandie als Kooperation der beiden Unispitäler in Lausanne (CHUV) und in Genf (HUG).
Das größte Lungentransplantationsprogramm im Kindes- und Jugendalter befindet sich in den USA am St. Louis Children's Hospital in St. Louis (Missouri).
In der Schweiz existieren zwei Zentren: dasjenige für die Deutschschweiz am Universitätsspital Zürich (USZ) und das Centre Romandie als Kooperation der beiden Unispitäler in Lausanne (CHUV) und in Genf (HUG).
Das größte Lungentransplantationsprogramm im Kindes- und Jugendalter befindet sich in den USA am St. Louis Children's Hospital in St. Louis (Missouri).
Indikationen
Die Indikation zur LTPL erfolgt im fortgeschrittenen Stadium einer Krankheit der Lungen oder des Lungenkreislaufes, nachdem alle konservativen Therapiemöglichkeiten maximal ausgeschöpft worden sind. In dieser Phase leiden die Patienten bereits bei der geringsten Anstrengung, teilweise sogar in Ruhe unter Luftnot (Dyspnoe) (NYHA-Klassifikation III-IV).
Die anzunehmende Lebenserwartung ohne Transplantation beträgt dann oft nur noch etwa 6 bis 18 Monate. Dies abzuschätzen ist im Einzelfall natürlich sehr schwierig und hängt vor allem auch von der zugrunde liegenden Krankheit ab. Dies sind vor allem die folgenden:

Indikationen
einschließlich Lungenemphysem bei Alpha-1-Antitrypsinmangel
einschließlich beidseitige Bronchiektasen
Man weiß aufgrund von Studien, dass bei COPD die Lebenserwartung nach Indikation zur Sauerstoff-Langzeittherapie, da heißt bei einem Sauerstoffpartialdruck <55 mmHg (<7,3 kPa), und einer Lungenfunktion mit einem FEV1 von 30 bis 40 % die Zweijahresüberlebensrate noch etwa 80 % beträgt. Ganz anders sieht es aber bei der Mukoviszidose aus, denn es muss bei diesen Patienten bei denselben oben erwähnten Werten eine LTPL unbedingt in Betracht gezogen werden.
Schwierig ist auch die Indikation bei pulmonaler Hypertonie, wo zum Beispiel die gemessenen Druckwerte im Lungenkreislauf für die Indikationsstellung zur LTPL keine entscheidende Rolle spielen.
Ein einfacher aber wichtiger Test, um die allgemeine körperliche Einschränkung abzuschätzen, ist der 6- beziehungsweise 12-Minuten-Gehtest, bei dem Transplantations-Kandidaten meist deutlich weniger als 400 beziehungsweise 600 Meter zurücklegen können.
Die obere Altersgrenze für eine Lungentransplantation beträgt zurzeit etwa 65 Jahre. Wichtiger als das chronologische Alter ist aber für die Entscheidungsfindung das biologische Alter, das heißt der Allgemein- und Ernährungszustand, das Fehlen von Störungen anderer Organsysteme sowie eine stabile psychosoziale Situation. Der ideale Zeitpunkt für die Transplantation ist deshalb oft schwierig festzulegen und hängt vor allem auch vom individuellen Krankheitsverlauf ab.
Insbesondere gilt es, den Moment zu erfassen, bei welchem sich der Zustand der Patienten rasch zu verschlechtern beginnt. Wichtige Hinweise dafür sind eine rasche Abnahme der Lungenfunktionswerte, ein zunehmender Sauerstoffgebrauch, wiederholte Rechtsherzdekompensationen, häufige Exazerbationen und Hospitalisationen, drohende Bettlägerigkeit und insbesondere beginnender Gewichtsverlust trotz optimaler Ernährung.
Der von der Stanford-Gruppe geprägte Begriff des „Transplantationsfensters“ illustriert sehr gut die Bedeutung dieser Überlegungen im Hinblick darauf, dass der Patient nicht zu früh, aber auch nicht zu spät für eine mögliche Lungentransplantation in Betracht gezogen wird. Bei vielen Patienten ist für die Entscheidung zur Transplantation vor allem die schwer eingeschränkte Lebensqualität, die ihnen das Leben nicht mehr lebenswert macht, ausschlaggebend.
Kontraindikationen
Absolute Kontraindikationen für eine LTPL sind mit den medizinischen Fortschritten der letzten Jahre selten geworden. Es sind dies vor allem schwere systemische Erkrankungen wie Sepsis, unbehandelbare Störungen der Blutgerinnung, schwere allgemeine Arteriosklerose oder Tumoren, die nicht länger als 5 Jahre erfolgreich behandelt sind. Funktionsstörungen anderer Organe wie chronisches Nierenversagen, Leberversagen oder Herzinsuffizienz sind heute relative Kontraindikationen, da bei solchen Patienten in ausgewählten Fällen auch eine kombinierte Transplantation, also zum Beispiel der Lungen und
Nieren, in Frage kommt. Als äußerst problematisch gilt hingegen eine Transplantation bei schweren Erkrankungen des Nervensystems, bei ernsthaften psychiatrischen Erkrankungen, sowie bei Missbrauch von Drogen, Alkohol oder Nikotin. Anders als früher führen heute die meisten Zentren eine LTPL auch in Fällen durch, bei denen bereits früher Operationen am Thorax durchgeführt worden sind oder die schwere Verwachsungen im Brustraum haben.

Technik der LTPL
Die Art der Transplantation hängt von der Grundkrankheit ab. Lungenkrankheiten, die mit chronischen Infekten einhergehen wie die Mukoviszidose oder Bronchiektasen, erfordern eine beidseitige LTPL. Bei allen übrigen Lungenkrankheiten kommt theoretisch eine Einzel-LTPL in Frage, sofern keine relevante Durchblutungsstörung der Lungengefäße mit Anstieg des pulmonalartiellen Blutdrucks (Pulmonale Hypertonie) vorliegt. Sie stellte bis vor kurzem die Methode der Wahl bei Lungenfibrose oder Lungenemphysem dar.
In den letzten Jahren hat sich aber gezeigt, dass bei der Transplantation von lediglich einer Lunge oft Probleme mit der verbleibenden anderen kranken Lunge entstehen wie zum Beispiel schwere Infektionen. Deshalb wird heute oft auch in diesen Fällen eine beidseitige LTPL durchgeführt. Dies hat auch den Vorteil, dass die Lungenfunktion nach der Transplantation deutlich besser ist. Der Nachteil ist jedoch, dass von einem Organspender nur ein statt zwei Patienten transplantiert werden können. Eine Herz-Lungentransplantation ist heute nur noch bei nicht korrigierbaren Herzfehlern mit Eisenmenger-Reaktion notwendig. Dies beruht auf der in den letzten Jahren gewonnenen Erkenntnis, dass sich auch bei schwerem Versagen des rechten Herzens bei pulmonaler Hypertonie dieses sich innerhalb weniger Tage bis Wochen vollständig erholt.
Die Technik der LTPL ist heute weitgehend standardisiert. Die Eröffnung des Brustraumes erfolgt heute meistens durch einen seitlichen Schnitt etwa zwischen der 8. und 9. Rippe. Nach der Entfernung der erkrankten Lunge werden zuerst die Bronchien, anschließend die Lungenvenen mit einem Stück des Herzvorhofes, und am Schluss die Lungenarterien der Spenderlunge mit den entsprechenden Strukturen beim Empfänger durch eine Naht verbunden. Bei der beidseitigen LTPL wird gleich anschließend nach der Transplantation der einen Lunge die andere mit derselben Technik verpflanzt. Oft kann dabei sogar ohne Herz-Lungenmaschine operiert werden, da während der Transplantation der ersten Lunge der Patient durch Beatmung der verbleibenden anderen kranken Lunge genügend mit Sauerstoff versorgt werden kann, und anschließend während der Ersetzung der zweiten Lunge die Beatmung dann bereits über die „neue“ Spenderlunge erfolgen kann.
Meist werden jedoch während der Operation Kreislaufunterstützungssysteme wie die ECMO (Extrakorporale Membranoxygenierung) eingesetzt oder bereitgehalten. Die Patienten werden bei komplikationslosem Verlauf meistens innerhalb von wenigen Stunden vom Beatmungsgerät entwöhnt und nach zwei bis drei Tagen von der Intensivstation auf die Normalstation verlegt. Im Rahmen der intensivmedizinischen Betreuung werden die ECMO und auch Dialysegeräte nach Bedarf eingesetzt. Anschließend erfolgt eine rasche Mobilisation unter intensiver physiotherapeutischer Betreuung. Die gesamt klinische Behandlung dauert etwa 3 Wochen. Der Verlauf ist vor allem bei Patienten mit pulmonaler Hypertonie etwas verzögert, und in 10–20 % kommt es zu Komplikationen, welche einen deutlich längeren Aufenthalt auf der Intensivstation und einen längeren Klinikaufenthalt notwendig machen.
Postoperative Komplikationen
In den ersten Wochen nach LTPL stellen chirurgische Probleme wie Blutungen, Lähmung des Zwerchfelles, Auseinanderklaffen oder Verengungen der Nahtstellen an den Bronchien und Lungengefäßen, akutes Lungen- oder Herzversagen sowie Infektionen die häufigsten Komplikationen dar. Nach dem ersten bis zum sechsten Monat sind es vor allem die akute Abstoßungsreaktion und Infektionen mit Bakterien, Viren und Pilzen. Im Langzeitverlauf, das heißt nach dem sechsten Monat nach LTPL, ist die wahrscheinlich in erster Linie auf einer chronischen Abstoßungsreaktion beruhende Bronchiolitis obliterans, beziehungsweise das Bronchiolitis-obliterans-Syndrom (BOS), die folgenschwerste Komplikation.
Die akute Abstoßungsreaktion nach LTPL ist heute dank der verbesserten Immunsuppression seltener geworden. Sie wird bei etwa einem Drittel der Patienten beobachtet, und einige machen zwei und mehr solche Episoden durch. Die akute Abstoßungsreaktion beruht auf einem Abwehrmechanismus des Körpers gegen das fremde Organ. Mikroskopisch findet sich im Gewebe eine Ansammlung von Entzündungszellen um die kleinen Lungengefäße. Während in den ersten 3–4 Wochen die Patienten dabei oft Fieber, Atemnot oder Veränderungen im Lungenröntgenbild haben, verläuft die akute Abstoßungsreaktion im weiteren Verlauf meistens ohne Symptome und kann nur aufgrund einer täglichen Kontrolle der Lungenfunktion und regelmäßiger transbronchialer Lungen-Biopsien, das heißt einer Gewebsprobenentnahme mittels Bronchoskopie, erfasst werden. Die akute Abstoßungsreaktion kann mit Gabe von hochdosiertem Kortison immer gut behandelt werden, stellt aber einen der wichtigsten Risikofaktoren für die spätere Entwicklung eines BOS dar.
Infektionen nach LTPL äußern sich meisten als Lungenentzündung. Aber auch Sepsis, Infekte des Magen-Darm-Traktes, der Nieren und Harnwege oder des Nervensystems kommen vor. Die häufigste Ursache sind verschiedene Bakterien, Viren (vor allem das Cytomegalievirus) sowie Pilze (Aspergillus fumigatus, Pneumocystis jirovecii). Durch eine gute Prophylaxe können diese Infektionen meistens verhindert, oder deren Schweregrad verringert werden.
Chronische Abstoßung
Ohne Zweifel ist das BOS die wichtigste und schwerwiegendste Komplikation nach LTPL. Es tritt über die Jahre bei bis zu 50 Prozent der Patienten auf und stellt ein Krankheitsbild dar, das gekennzeichnet ist durch eine zumeist langsam beginnende, aber leider in vielen Fällen unaufhaltsam fortschreitende Verschlechterung der Lungenfunktion.
Histologisch manifestiert sich das BOS durch Vernarbung und schließlich Zerstörung der Bronchiolen sowie Pfröpfen von Gewebe in den kleinen Atemwegen und Alveolen. Da jedoch die transbronchiale Lungenbiopsie oft unergiebig ist, wird die Diagnose aufgrund der Lungenfunktion gestellt. Beim BOS kommt es zu einer Verschlechterung des FEV1 im Vergleich zum Durchschnitt der zwei besten postoperativ gemessenen Werte. Folgende Stadien des BOS werden unterschieden:
.jpg)
- Stadium 0 FEV1 >90 % des Ausgangswertes
- Stadium 0-p FEV1 81–90 % des Ausgangswertes
- Stadium 1 FEV1 66–80 % des Ausgangswertes
- Stadium 2 FEV1 51–65 % des Ausgangswertes
- Stadium 3 FEV1 < 50 % des Ausgangswertes
Die Ursache des BOS ist nicht ganz geklärt. Die meisten Autoren sind der Meinung, dass es sich dabei um eine Form einer chronischen Abstoßungsreaktion handelt, welche möglicherweise Folge von verpassten beziehungsweise nicht behandelten akuten Abstoßungsreaktionen ist. Heute ist man aber der Auffassung, dass viele andere Faktoren wie
wiederholte Infekte oder nicht erkannte nächtliche Aspiration von Magensaft (gastroösophagealer Reflux) eine wichtige Rolle spielen. Ein Zusammenhang mit dem Cytomegalievirus wird immer wieder diskutiert, konnte aber bisher nicht eindeutig nachgewiesen werden. Am häufigsten tritt das BOS 1–2 Jahre nach LTPL auf. Beginnt es später, ist
wohl die häufigste Ursache eine mangelhafte Compliance der Patienten, das heißt eine unzuverlässige Einnahme der Medikamente.
Die Prophylaxe des BOS besteht vor allem in der frühzeitigen Diagnose und Behandlung von akuten Abstoßungsreaktionen, in der konsequenten Vorbeugung und Behandlung von Infektionen, in Maßnahmen gegen den gastroösophagealen Reflux, und der intensiven Betreuung und Motivation der Patienten zur Verbesserung der Medikamenten-Compliance. Die Behandlung eines bereits bestehenden BOS ist schwierig. In etwa 1/3 der Fälle kann mit vermehrter Immunsuppression eine Besserung erreicht werden. Ein Drittel der Patienten zeigt einen stationären Verlauf. In einem weiteren Drittel kommt es jedoch zu einer anhaltenden, nicht beeinflussbaren Verschlechterung der Lungenfunktion, so dass schließlich nur noch eine erneute Transplantation in Frage kommt.
Quelle: Wikipedia.de - Lungentransplantation 2021